- HOME
- 本プログラムについて
- ターゲットタンパク研究「基本的な生命の解明」分野
- ストレス応答生体防御センサー
発癌性物質や酸化ストレスに応答する生体防御系センサーの構造基盤
代表機関:東北大学大学院医学系研究科
代表研究者:山本雅之
2010年版パンフレット(背景と成果)の該当ページはこちら
癌や動脈硬化、糖尿病などの原因の一つとして、毒性化学物質が細胞を傷つけることがあげられます。ここでいう毒性化学物質とは、他の分子から電子を奪う性質をもった「親電子性分子」や、酸素からできる「活性酸素」のことで、細胞中の遺伝子DNAに直接作用して変異を引き起こします。いずれも、食物や大気に含まれているので、日々の生活を営む以上、体内への取り込みは避けられません。つまり、私たちは常にその危険にさらされているのです。
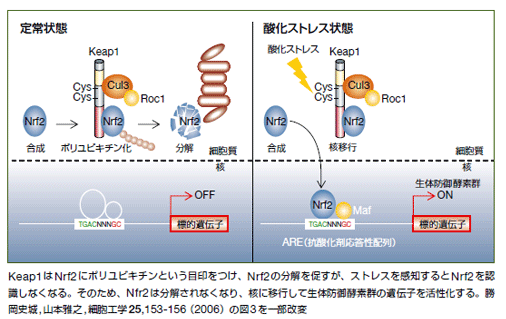
しかし、ヒトの体は、こうしたストレスを感知して、無毒化する「しくみ」を備えています。私たちは、このしくみに関係するタンパク質の解析に、これまで取り組んできました。中でも、中心的な役割を担っているのが、親電子性分子や活性酸素ストレスを感知するセンサータンパク質Keap1です。このタンパク質は細胞質にあって、ストレスのないときはNrf2という転写因子のはたらきを抑えています。しかし、Keap1がストレスを感知するとその抑制は解かれ、Nrf2は活性化して細胞質から核へ移動します。そして、Nrf2はストレスから身を守るために必要な抗酸化酵素群や解毒酵素群の遺伝子を発現させる(遺伝子DNAの情報をもとに酵素をつくらせる)のです。
とはいえ、Keap1が親電子性分子や活性酸素のような多様なストレス分子を感知して、ストレス状態にあることを細胞内に伝える詳しい分子機構はまだ解明されていません。ストレスのないとき、Keap1はNrf2の分解を促すことでその活性を抑えています。その詳しい機構を知るには、Keap1とNrf2の複合体の構造を解析することが必要です。また、Nrf2が遺伝子を発現させるときには、別の転写因子も加わります。Nrf2とその転写因子とDNAの複合体の構造も解析して、特定の遺伝子が発現するしくみを解明したいと思っています。さらに、マウスを使ってこれらのタンパク質の機能を調べることを計画しています。
最近の研究から、このストレスに対する応答機構が適切にはたらかなくなると抗癌剤が効きにくくなる場合があることがわかってきました。肺癌患者のKeap1には変異が多く、Nrf2のはたらきを抑えることができません。つまり、ストレス応答系が常に活性化されているのですが、そのために薬剤耐性を示す遺伝子も活性化され、抗癌剤が効きにくくなるのです。私たちの研究でNrf2の阻害剤を見つけることができれば、抗癌剤と併用することにより、この問題を解決できる可能性もあります。これに限らず、Keap1-Nrf2制御システムをタンパク質の構造という視点から精密に理解できれば、将来の疾患予防につながることでしょう。

 サイト内検索
サイト内検索